لایهی SEI در باتری لیتیوم یون (قسمت اول)
باتری لیتیوم یون یک باتری شارژ پذیر است که درون آن واکنشهای بسیاری رخ میدهد که این واکنشها از پیچیدگی بالایی برخوردارند. برای مشخص شدن کامل این واکنشها مطالعات زیادی باید انجام گیرد تا جزئیات واکنشهای جانبی در باتری لیتیوم یون، مشخص گردد. لایهی SEI یک لایهای است که به دلیل واکنشهای جانبی درون باتری ایجاد میشودکه خود مزایا و معایب خاص به خود را دارد.
لایهی SEI چیست
همانطور که میدانیم هر مادهای در یک محدوده پتانسیلی پایدار است و کمتر و بیشتر از این محدوده دچار فرآیند احیا یا اکسایش میشود. در هنگام شارژ باتری نیز درست مثل تجزیه آب، ما انرژی را از طریق شارژر به باتری میدهیم تا عکس واکنشی که در باتری انجام میشد صورت بگیرد و باتری به حالت قبل از تخلیه برگردد.
الکترولیت آلی که در باتری یون لیتیومی استفاده میشود (همانند الکترولیز آب) در نتیجه انرژی ناشی از شارژر، دچار تغییر میشود. همانطور که بیان شد در یک باتری یون لیتیومی، در قطب منفی (آند گرافیتی) در حین شارژ احیای یون لیتیوم صورت میگیرد.
با توجه به اینکه تمایل به احیای الکترولیت از نظر ترمودینامیکی بیشتر از یون لیتیوم است، بنابراین احیای الکترولیت بهجای احیای یون لیتیوم صورت میگیرد. این اتفاق باعث میشود بر روی سطح گرافیت یک لایه جامد ایجاد میشود. این لایه جامد اصطلاحا لایهی SEI مخفف (Solid Electrolyte Interface) نامیده میشود.
” بیشتر بخوانید: راهکارهای افزایش طول عمر باتری لیتیومی “
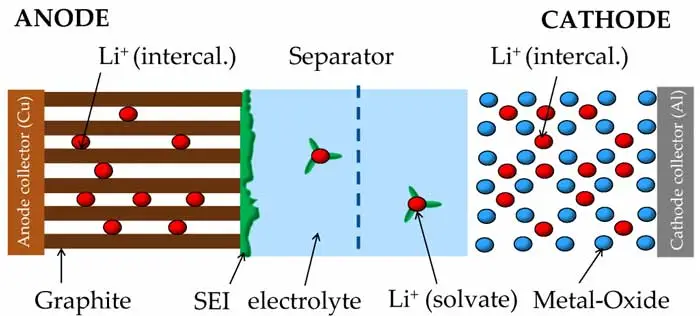
ترکیب لایهی SEI
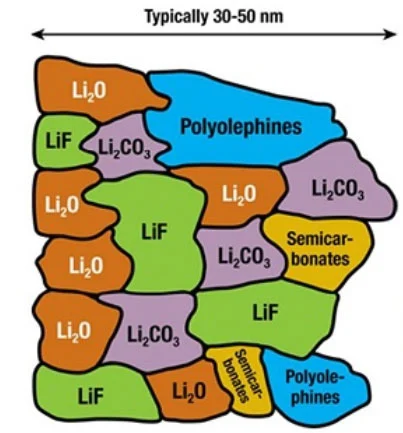
ترکیب این لایه پیچیده و مخلوطی از چندین ماده شیمیایی است. شکل زیر شماتیک این لایه را نشان میدهد. همانطور که از روی شکل مشخص است، ترکیب این ماده دارای یون لیتیوم است؛ بنابراین تشکیل این لایه با کم شدن لیتیوم همراه است که موجب کاهش ظرفیت در اولین مرتبه شارژ میشود. این لایه ضخامتش همانطور که در شکل زیر نشان داده شده است، در محدوده نانومتری است. بررسی و تحقیق بر روی ترکیب SEI و مکانیزم تشکیل یکی از مباحث مورد بررسی در مقالات پژوهشی است.
” بیشتر بخوانید: لایهی SEI (قسمت دوم) “
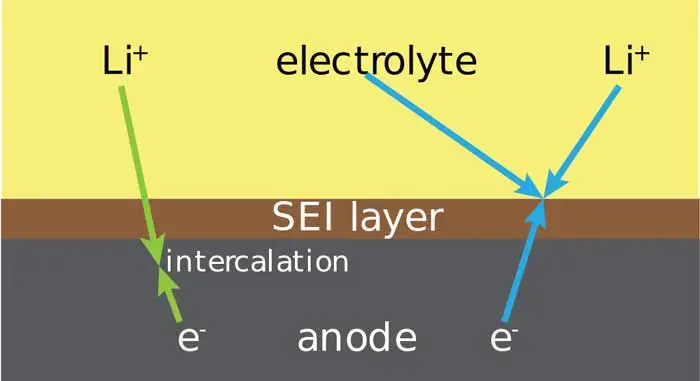
تاثیر لایهی SEI بر باتری
تشکیل لایه SEI، خودش ادامه واکنش احیای الکترولیت را محدود میکند. چون بهصورت یک مانع فیزیکی از رسیدن مولکولهای الکترولیت به سطح آند جلوگیری میکند. در واقع به صورت یک مانع عمل میکند (همانند لایه غیر فعال اکسید آلومینیوم که از رسیدن اکسیژن به آلومینیوم زیرین جلوگیری میکند و از اکسید شدن بقیه آلومینیوم ممانعت به عمل میآورد).
لایهی SEI یک عایق الکتریکی است که از رسیدن الکترون به الکترولیت جلوگیری میکند و در این صورت نه الکترون میتواند به سمت مولکول الکترولیت برسد و نه مولکول الکترولیت به سمت الکترون موجود در آند حرکت کند که هر دو موجب میشوند احیای الکترولیت دیگر صورت نگیرد و یک واکنش خود محدود شونده داشته باشیم.
نکتهی جالب برای لایهی SEI این است که این لایه برای یون لیتیوم نفوذپذیر است و یون لیتیوم میتواند از آن عبور کند و به سطح آند برسد و الکترون بگیرد و احیا شود. پس این لایه برای باتری لیتیوم یون میتواند مفید واقع شود اما از طرفی این لایه چون مسافت نفوذ یون لیتیوم را برای رسیدن به آند زیاد میکند توان باتری را کاهش میدهد که در باتریهای توان بالا باید به این نکته توجه ویژه گردد.
" بیشتر بخوانید: SEI ارتقا یافته در باتریهای لیتیوم یون "
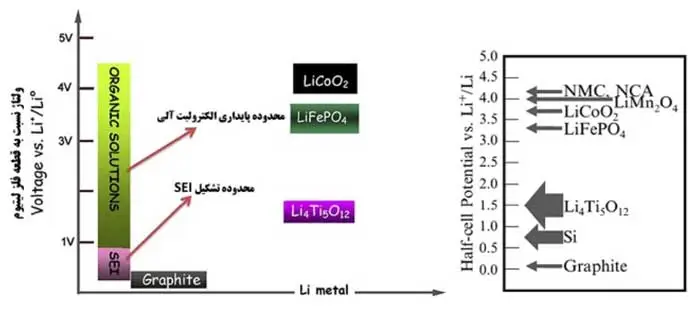
شکل زیر محدوده پایداری الکترولیت را در مقابل پتانسیل آندها و کاتدها نشان میدهد. اگر کاتدی دارای پتانسیل بالاتر از محدوده پایداری الکترولیت باشد، در کاتد و در هنگام شارژ، الکترولیت اکسید میشود و همینطور اگر آند دارای پتانسیل پایینتری از محدوده پایداری باشد، در آند و در هنگام شارژ الکترولیت احیا میشود. خوشبختانه همانطور که در شکل زیر مشاهده میشود، کاتدهای معمول مشکل ناپایداری الکترولیت را ندارند ولی در آند گرافیتی و سیلیکون ناپایداری وجود دارد و SEI تشکیل میشود.
منبع: edu.nano.ir
ویراستار: حسین جعفری پور











